在我们的体内,衰老细胞是衰老的“关键操控者”,决定着身体走向衰老的速度。这些细胞随着年龄的增长而逐渐积累,它们不再正常分裂,丧失了原有的功能,并且开始分泌一系列有害物质。这些衰老细胞被认为是引发衰老和多种疾病的“罪魁祸首”,如心血管疾病、糖尿病、关节炎和神经退行等疾病。
近期,中国科学院分子细胞科学卓越创新中心的一项开创性的研究发现,通过激活VEGF信号通路,可以改善内皮细胞的功能,减少肝脏中的老化现象。这一发现为针对不同衰老细胞类型的精确治疗提供了理论基础。这项研究为清除衰老细胞分泌的有害细胞提供了新的希望,让我们看到了治疗相关疾病甚至延缓衰老的可能。

实验设计与过程
研究人员首先创建了一种特殊的小鼠模型,其可以在小鼠体内的p16Ink4a细胞上标记一个“荧光标签”。p16Ink4a是一种广泛认可的衰老细胞标志物,它的表达通常与细胞的衰老状态密切相关。通过这种方法,研究人员能够实时追踪和观察这些衰老细胞在不同器官中的分布和行为。
在实验中,研究人员对小鼠进行了化学损伤,以模拟人类肝脏损伤的情况。这种损伤导致肝脏中出现大量衰老细胞,这些细胞被“荧光标签”标记,从而使得研究人员能够清晰地观察到它们。他们发现,在受损的肝脏中,标记了荧光的衰老细胞主要是巨噬细胞和内皮细胞。这些细胞在肝脏修复过程中发挥了重要作用,但它们的积累也导致了肝脏功能的下降。
为了测试是否可以通过改变这些细胞的行为来改善肝脏损伤,研究人员采用了基因工程技术。他们创建了一种新的小鼠模型,能够特异性地在内皮细胞中过表达一种叫做Kdr的基因。Kdr基因编码的蛋白质是血管内皮生长因子受体,对血管生成和修复至关重要。
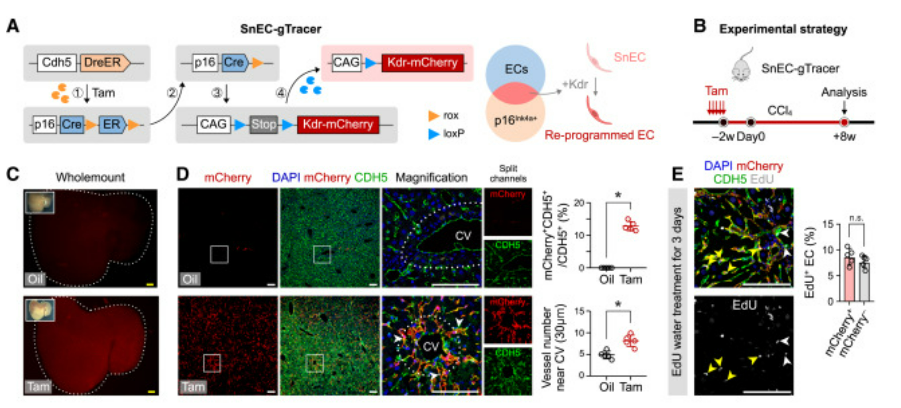
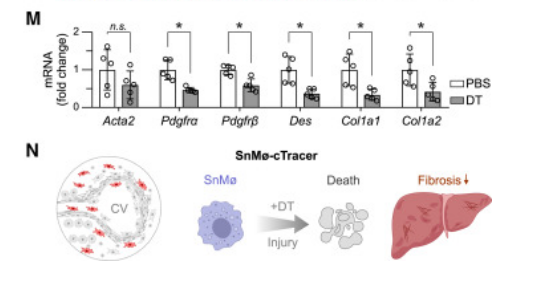
实验结果显示,通过表达Kdr基因,内皮细胞在受损肝脏中的数量增加,新血管的形成也显著提高。这一发现具有重要意义,新血管的生成对于受损组织的修复至关重要。更重要的是,这种基因操作减少了肝脏中的纤维化区域,纤维化是肝脏损伤长期无法修复的后果,也是肝硬化等严重疾病的主要特征。
这些发现表明,通过特定的基因编程,我们或许能够清除或改造衰老细胞,从而在一定程度上延缓衰老进程,治疗与衰老相关的疾病。研究人员进一步分析了这些基因改造细胞的具体作用机制,发现它们不仅促进了血管生成,还减少了炎症反应,提高了组织的再生能力。
对未来研究的展望
传统的衰老细胞清除策略通常是“一刀切”的方式,但新的研究表明,这种做法可能并非最佳。针对巨噬细胞和内皮细胞的不同功能,研究人员提出了更为精细的治疗策略。未来的研究将致力于以下几个方向:
1.细胞类型特异性清除:开发能够特异性识别和清除特定衰老细胞类型的方法。
2.分子机制的解析:深入理解衰老细胞的功能和它们在衰老过程中的作用。
3.临床应用的探索:将实验室的研究成果转化为临床上的有效治疗手段。
参考文献:Zhao H,Liu Z,Chen H,et al.Identifying specific functional roles for senescence across cell types.[J].Cell,1970,25:7314-7334.e21.